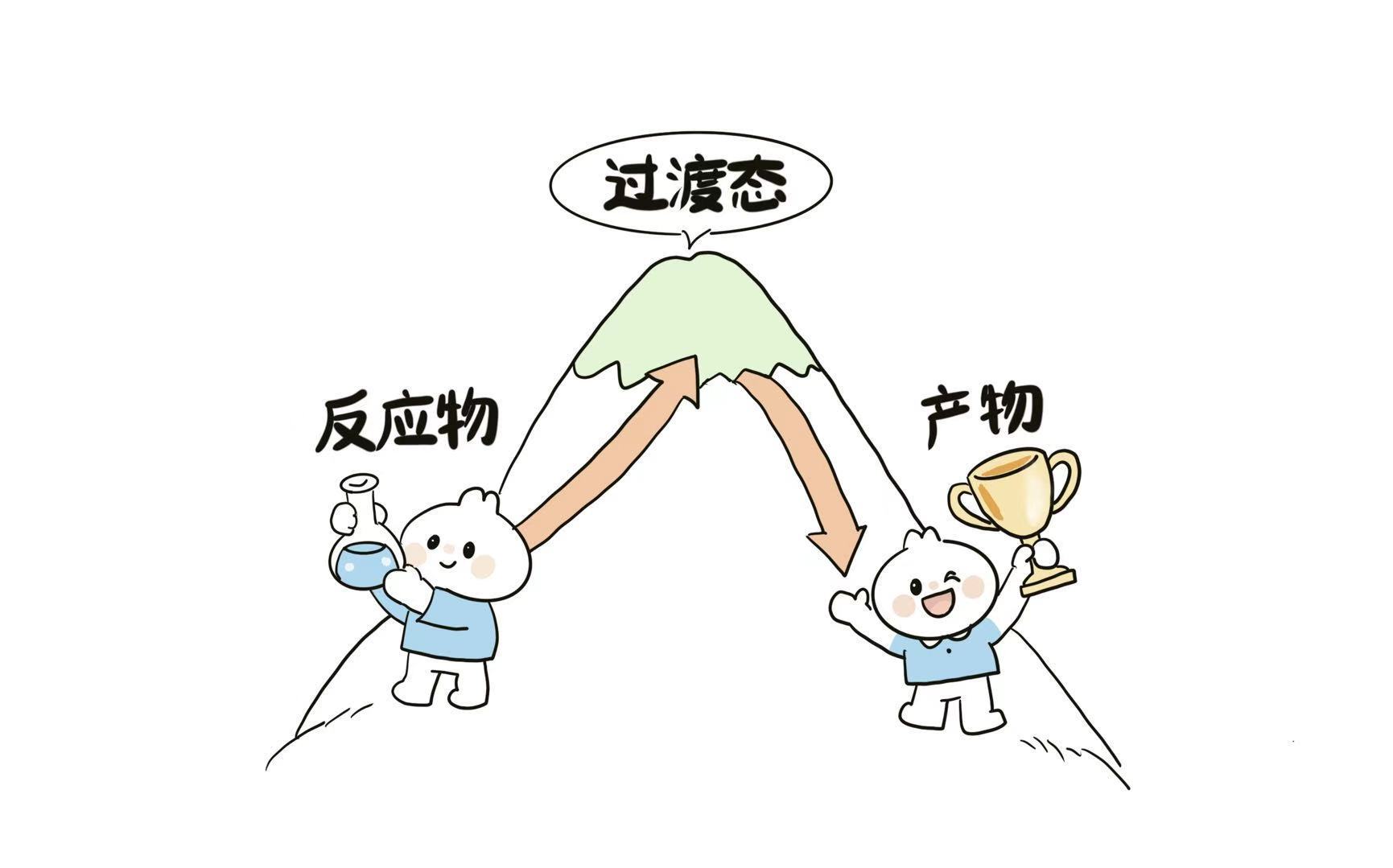
当化学反应发生时,反应物并不会直接变成产物,而是必须经过一个局域能量最高、极不稳定的中间状态——这就是过渡态。你可以把它想象成翻越一座山峰:山脚下是反应物,另一侧山脚下是产物,而山顶就是过渡态。要想从一边到达另一边,通常需要经过这个能量“山顶”。
过渡态的生命周期往往极其短暂,通常只有飞秒(10⁻¹⁵秒)量级,无法被分离或直接观察。但它决定了反应发生的快慢甚至反应是否能够发生——能量“山顶”越高,反应就越困难、越缓慢;反之,则越容易进行。
近年来,科学家对过渡态有了更进一步的理解,分子反应动力学研究揭示,反应实际经历的是动力学的过渡态,它与反应的初始量子态直接相关;此外,“漫游”机制能够为反应提供一条低能量通道,使其能够绕过高能量的传统过渡态。
另外,科学家还通过理论计算和实验技术结合来“捕捉”过渡态的“蛛丝马迹”。理解过渡态的结构和性质,能够更加有针对性地制备反应物或设计催化剂——尽量降低反应“山峰”的“高度”,让反应轻松加速。因此,过渡态理论成为现代化学、生物化学和材料科学中理解与调控反应过程的重要工具之一。(文/刘舒 图/陈思)