近日,我所微流控芯片研究组(1807组)秦建华研究员团队受邀发表综述文章,系统总结了该团队在利用器官芯片开展感染性疾病研究方面的一系列成果,并对该领域的未来发展进行了展望。
感染性疾病多指由各种常见病原体(如细菌、真菌、病毒和寄生虫等)引起的机体疾病,可引起人体全身性病理症状,严重者可导致高发病率和死亡率。例如,20世纪流感病毒引发H1N1等多次疫情;2002年冠状病毒SARS引发的急性呼吸道传染病;2019年出现的新型冠状病毒(SARS-CoV-2),已导致全球大流行,严重威胁人类健康。目前,针对感染性疾病研究模型主要依赖于细胞和动物试验,但这些实验模型在不同程度上仍存在一定局限。在单层细胞上的病原体培养方式往往缺少体内复杂动态的组织微环境和机体免疫反应,动物模型则由于存在物种差异,难以反映人体的真实反应。因此,建立能准确反映人类病理生理特征的新型实验模型体系,对于感染性疾病机制研究及有效诊疗等具有重要意义。
器官芯片是近年发展起来的一种前沿交叉科学技术,它融合了物理、化学、工程学和生物学等多学科方法,可在体外模拟包含多细胞组成,组织-组织界面,机械流体等多因素的复杂细胞微环境,反映组织器官的关键结构与功能特点,在疾病模型、机理研究和新药研发等方面具有重要应用潜力,也为感染性疾病研究提供了新策略和新方法。
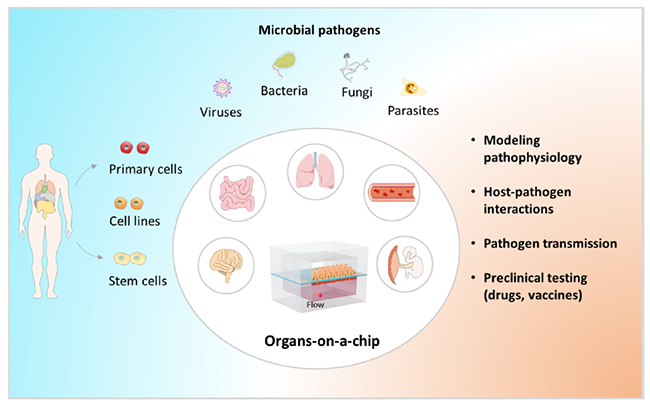
本综述首先概述了器官芯片应用于病原体感染研究的最新进展,通过一些代表性实例向读者展示了利用该技术开展病原-宿主相互作用研究的特点和技术优势。例如,血管组织模型用于模拟研究埃博拉病毒感染引起的出血性综合征;肝组织芯片用于研究乙肝病毒感染,并呈现出近体内的生物学反应等。针对新冠肺炎的暴发,秦建华团队率先利用器官芯片技术开展了新冠病毒对肺组织和肠组织感染研究:利用自行构建的三维肺泡组织和肠组织感染模型,揭示了新冠病毒感染导致人肺泡-毛细血管屏障和肠组织损伤的主要病理特征,并探讨了外周免疫细胞介导病毒感染导致的炎症反应和组织屏障功能障碍的潜在机制(Advanced Science,2020;Science Bulletin,2021;Cell death & Disease,2020)。基于器官芯片的体外模型,可在组织器官水平反映新冠病毒感染中多细胞复杂因素参与的病原-宿主相互作用。更重要的是,器官芯片可见证细胞间相互作用以及免疫细胞介导的炎症过程,并可延伸用于多器官累及的复杂感染性疾病研究,为病毒感染致病机制和药物发现等提供了新型实验体系。
此外,秦建华团队还尝试了利用器官芯片研究由细菌导致的常见感染性疾病。例如,孕期宫内感染,包括病原菌及其引起的相关炎症反应是导致早产或流产的重要危险因素,目前尚缺乏研究早期宫内感染的体外模型。秦建华团队利用人源性胎盘细胞和干细胞,建立了三维动态的胎盘屏障和羊膜组织模型,研究宫内细菌感染导致的胎盘炎症和绒毛膜羊膜炎等疾病。这些工作为加深认识和理解宫内感染及其不良妊娠结果,寻求有效治疗策略等提供了新的思路。最后,综述探讨了开发新一代人类器官病理生理模拟系统的迫切性和面临的挑战,这将为重大感染性疾病研究以及极端条件实验等提供新的技术平台。
近年来,秦建华团队主要致力于器官芯片、干细胞衍生类器官及其与生命科学的前沿交叉研究,系统建立了一系列具有人体生理关联性的体外组织和类器官模型体系,探究组织器官发育及相关疾病机制,为在系统层面开展医学研究和药物发现等提供新的策略和思路。
该综述以“Microfluidic Organs-on-a-Chip for Modeling Human Infectious Diseases”为题,发表在《化学研究评述》(Accounts of Chemical Research)上。(文/图 王亚清)






