近日,我所分子模拟与设计研究组(1106组)李国辉研究员团队与清华大学药学院尹航教授团队合作,揭示了ZDHHC18介导的cGAS棕榈酰化修饰抑制先天免疫的分子机制。
环状GMP-AMP合酶(cGAS)是一种双链DNA(dsDNA)传感蛋白,在病原体来源的核酸诱导强有力的先天免疫反应中发挥着重要的生物学功能。当cGAS感知微生物病原体的dsDNA入侵时,通过2:2 cGAS/DNA复合物的形式将ATP与GTP催化合成环状二核苷酸cGAMP,所产生的cGAMP通过STING-TBK1-IRF3信号轴介导I型干扰素的诱导,进而引发天然免疫反应。
大量的研究认为cGAS活性的改变与先天免疫反应沉默(cGAS过度抑制)和自身免疫性疾病(cGAS过度激活)的发生息息相关。因此,必须对cGAS活性进行良好调节,防止过度抑制(导致先天免疫反应沉默和病原体入侵)和过度激活(可能导致自身免疫或慢性炎症疾病)。尹航团队实验发现了棕榈酰转移酶ZDHHC18可以通过棕榈酰化cGAS的C474位点来抑制cGAS与DNA结合和2:2 cGAS/DNA复合物的形成,从而抑制cGAS的过度激活,为负向调控cGAS生物学活动提供了新的研究策略。但是仅依据实验无法从分子层面阐明棕榈酰化如何调控cGAS的活性。
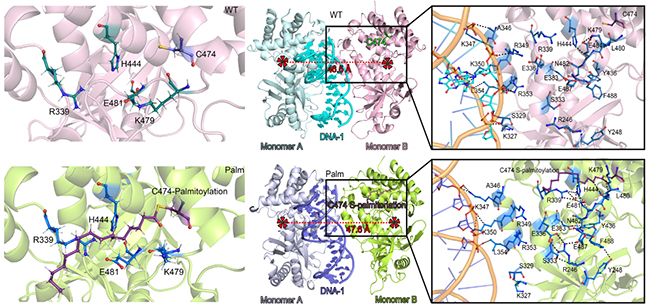
为了揭示棕榈酰化调控cGAS活性的分子机制,李国辉团队运用分子动力学模拟的方法,针对野生型和棕榈酰化修饰的2:2 cGAS-DNA复合体进行大规模理论计算研究,发现cGAS的C474棕榈酰化导致E481侧链发生了明显的翻转,促使原本与K479形成相互作用的E481与R339和H444发生相互作用,进而增强了S329-L354,F433-P450和E478-S493的相互作用。这些相互作用的改变促使位于monomer B上的R236、R255、K327、S329、K347、R349、K350、R353和L354远离DNA1,通过削弱DNA在2:2 cGAS-DNA复合体中的桥梁作用来降低两个1:1 cGAS-DNA复合体之间的二聚化程度,最终抑制了cGAS的过度激活。该工作发现,cGAS的棕榈酰化修饰是一种新的先天免疫反应的抑制机制,为抗病毒感染和自身免疫性疾病的药物开发提供潜在的靶点。
相关成果以“ZDHHC18 Negatively Regulates cGAS‐mediated Innate Immunity through Palmitoylation”为题,于近日发表在The EMBO Journal上。该工作的共同第一作者是我所1106组刘野助理研究员,上述工作得到国家自然科学基金、国家重点研发计划等项目的支持。(文/图 刘野、楚慧郢)






