近日,我所微流控芯片研究组(1807组)秦建华研究员团队利用人诱导多能干细胞(hiPSC)建立了一种三维培养体系,可在体外形成具有血管样结构的胎盘类器官,模拟人早期胎盘的发育特征。
胎盘是妊娠期维持母体和胎儿健康的一个重要器官,具有营养物质转运、代谢和分泌等生理功能。人类胎盘主要由多种类型的滋养层细胞和血管内皮细胞等组成。目前,能够用于研究人类胎盘发育和功能的体外模型仍然缺乏,因此,开发建立具有高度生理相关性的胎盘模型对于母胎医学和胎盘相关疾病研究至关重要。
前期,秦建华团队利用生物学和工程学协同策略,将细胞自组织与器官芯片技术相结合,在体外建立了hiPSC衍生的滋养层样组织3D模型,可模拟人早期胎盘的发育特征,并研究探讨了流体力学因素对胎盘组织分化和分泌功能的影响 (Advanced Science,2022;Frontiers in Bioengineering and Biotechnology,2022)。尽管目前胎盘类器官可在一定程度上反映人类胎盘的组织结构和功能特征,但由于胎盘在体内是一个高度血管化的器官,如何在体外建立具有血管结构特征的胎盘类器官,更真实模拟体内的复杂微环境,仍然是该领域面临的挑战和难点。
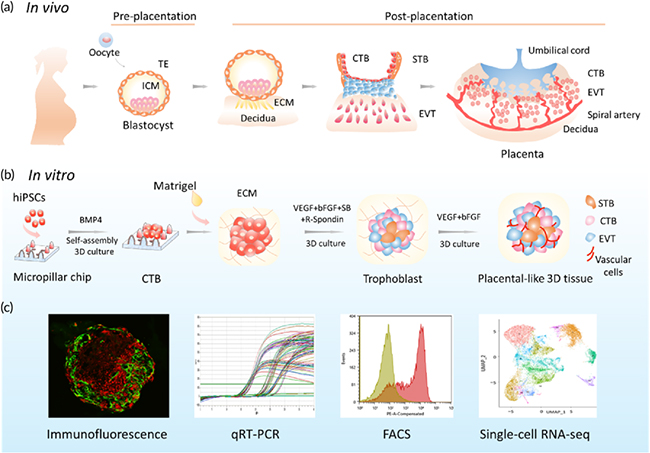
本工作中,该团队优化建立了一种包含特定生长因子和细胞外基质的3D培养体系,通过诱导hiPSC向滋养层细胞和血管内皮细胞进行多向分化,形成具有血管样结构的胎盘类器官。经过免疫荧光、流式细胞分析、实时定量PCR等鉴定,所产生的胎盘类器官具有类似妊娠早期人类胎盘的一些关键特征,其中包含主要的滋养层细胞类型,如细胞滋养层、合体滋养层细胞和侵润型绒毛外滋养层以及内源性血管内皮细胞等。此外,该类器官还具有微绒毛结构,并可分泌胎盘特异性激素(hCG-β)和血管内皮生长因子A(VEGFA)等。团队通过单细胞转录组分析证实,所形成的滋养层类器官与人早孕胎盘组织的表型特征具有高度相似性。进一步研究发现,胎盘类器官对炎性因子(TNF-α)和VEGF受体抑制剂的刺激产生响应,可模拟体内胎盘组织的生理、病理特征。新构建的胎盘类器官模型包含多种滋养层细胞亚型、血管样结构和组织关键功能特征,为研究人类早期胎盘发育、先兆子痫和病原体感染等提供了新思路。
相关工作以“Engineering placenta-like organoids containing endogenous vascular cells from human-induced pluripotent stem cells”为题,发表在Bioengineering & Translational Medicine上。上述工作得到中科院B类先导专项“面向病原体—宿主相互作用研究的器官芯片新技术、新方法”、国家自然科学基金等项目的支持。(文/图 王亚清)






