近日,我所生物技术研究部生物分离与界面分子机制研究组(1824组)卿光焱研究员团队与中药科学研究中心(2800组群)梁鑫淼研究员团队合作,在中性糖链结构解析方面取得新进展。合作团队通过对糖链进行衍生化标记的策略,利用纳米孔的突变,实现了对基于蛋白纳米孔的糖链精确结构的解析,并揭示了糖链分子与纳米孔界面相互作用机制。
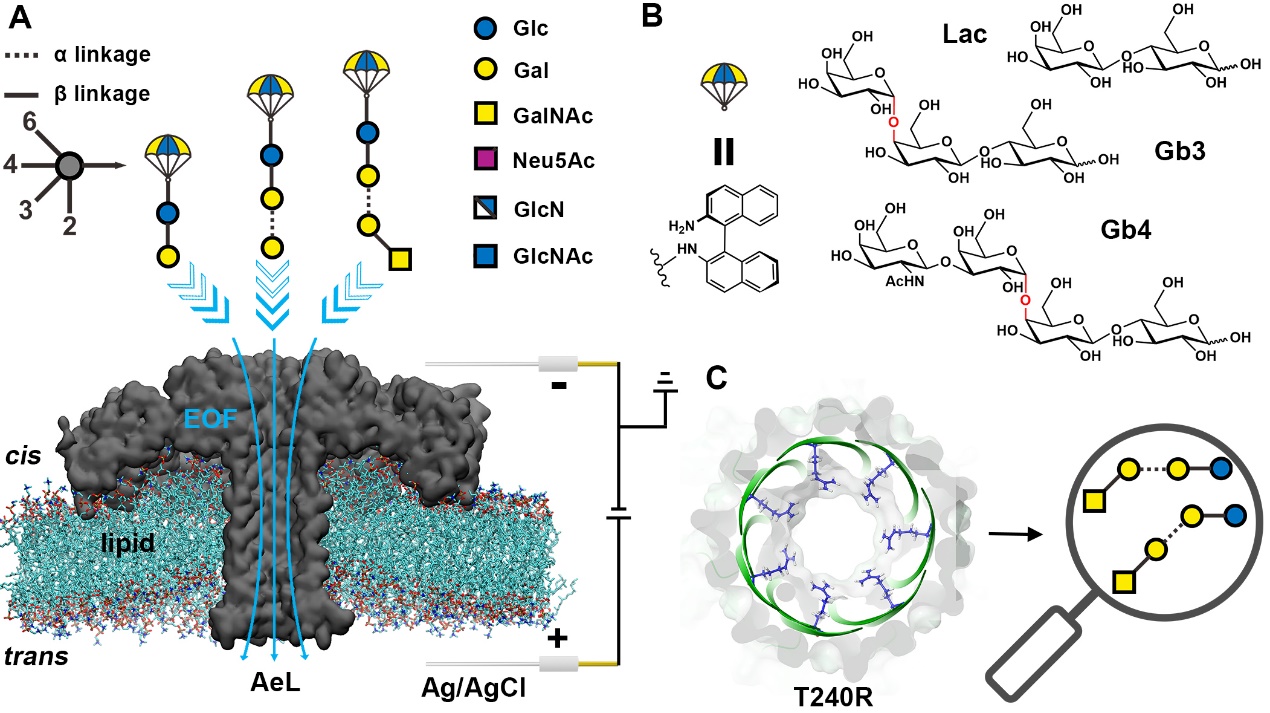
迄今为止,科研人员研究的绝大多数物种的细胞表面都“覆盖”一层“糖被”,此外,超过一半的蛋白都会进行糖基化修饰。因此,糖链在生物体的生理和病理过程中都担任着重要角色。然而,由于糖链本身的结构异质性,包括复杂的单糖组成、序列、连接类型、分支结构、和异构立体化学等,难以对其结构进行精准解。此外,大多数糖链本质上是中性的,电离效率低,且中性糖链仅具有羟基官能团,缺乏电荷,抑制了它们与纳米孔相互作用的能力,难以被纳米孔所传感。这限制了中性糖链的分析手段,也阻碍了糖组学的发展,导致目前科研人员对中性糖链在生物体内发挥怎样的生物学功能缺乏更多、更深入的了解。因此,亟需开发一种高效、简便的中性糖链的精细结构解析方法。
本工作中,卿光焱团队在前期基于稳态离子电流的固态纳米孔道传感策略实现唾液酸糖链异构体区分(Chem. Sci.,2020)、基于瞬态离子电流的纳米孔传感策略实现唾液酸糖链的结构分析(Nat. Commun.,2023)等工作的基础上,设计开发了以联萘作为标签的糖链衍生化策略,增强了衍生化糖链分子与纳米孔界面之间的阳离子-π相互作用,降低了糖链分子过孔的易位速度,从而实现了利用气溶素(AeL)纳米孔检测中性糖链。该方法可以通过单糖/基团分辨率来区分不同糖链,并且具有监测酶转糖基化反应的潜力。卿光焱团队对AeL纳米孔进行突变改造后,得到的突变体T240R可实现对六种二糖异构体,以及三糖和四糖连接异构体的明确鉴定。此外梁鑫淼团队开展了机器学习和分子对接工作,利用机器学习实现了多样品区分及混合样品占比预测,并通过分子对接模拟,揭示了纳米孔内壁氨基酸残基(R282、K238、R240)与糖链/联萘标签相互作用模式。更重要的是,本工作演示了中性糖链异构体的动力学易位过程,为基于纳米孔的糖链分析奠定了理论基础。该工作有望促进糖链结构异构体的分析,并为基于纳米孔的糖链结构测定和测序提供新思路。
相关研究以“Precise structural analysis of neutral glycans using aerolysin mutant T240R nanopore”为题,于近日发表在《美国化学学会-纳米》(ACS Nano)上。该工作的第一作者是1824组博士研究生逯文启和助理研究员赵新佳。上述工作得到了国家自然科学基金、国家重点研发计划、我所创新基金等项目的资助。(文/图 逯文启、赵新佳)






