近日,我所生物技术研究部分子探针与荧光成像研究组(1818组)徐兆超研究员、乔庆龙副研究员团队,与华东理工大学郭志前教授、新加坡科技设计大学刘晓刚教授合作,在生物医学成像领域取得新进展,提出了一种基于噁唑啉开关(Oxazolidine Switch)的“荧光缓冲”策略,克服了近红外Cy7菁染料光稳定性不足的难题。该策略无需改变Cy7母体结构,即可提升其光稳定性,有望为荧光引导手术、肿瘤长期追踪、细胞超分辨成像等领域提供一种更安全、更可靠的工具。
Cy7染料因其近红外光穿透性强、生物相容性高,已被广泛应用于肿瘤边界可视化、淋巴示踪等手术导航场景中,并成为美国FDA批准的临床级造影剂(例如吲哚菁绿ICG)。然而,传统Cy7染料在光照下极易发生光漂白,限制了其在长时间手术及活体动态监测中的应用。尽管近年来不断有新型近红外染料问世,但其临床安全性验证通常需要超过10年,难以满足快速应用需求。
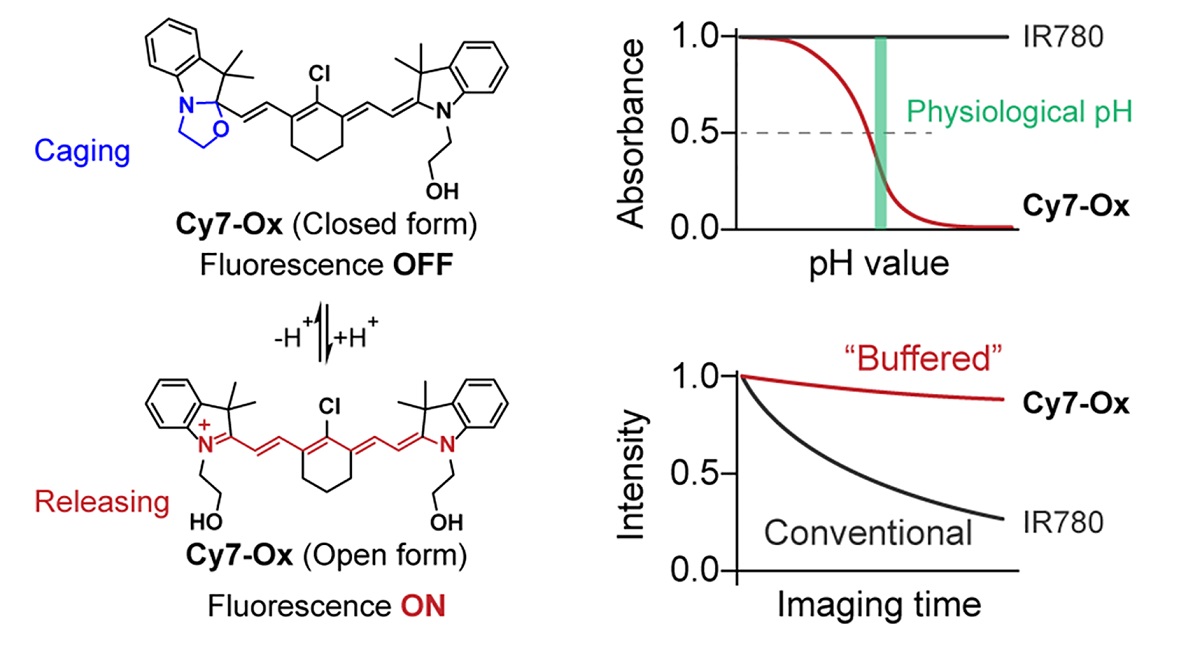
本工作中,合作团队希望赋予“老药”新生,在不改变Cy7临床安全性的前提下,增强其抗光漂白能力。团队创新性地设计了一种[2,1-b]噁唑烷开关修饰的Cy7探针(Cy7-Ox),巧妙利用“闭环(非荧光)-开环(荧光)”的动态平衡,使染料具备“自修复”功能。Cy7-Ox探针在靶标区域(例如肿瘤组织)发生光漂白时,周围未激活的闭环分子会迅速转化为荧光态,实时补充荧光信号,从而维持稳定成像。此外,该策略完整保留Cy7母核结构,避免了传统化学修饰可能带来的生物毒性风险。在小鼠肿瘤活体成像实验中,Cy7-Ox的荧光信号可稳定超过30分钟,大幅提升了近红外成像的光稳定性。
相关研究成果以“Oxazolidine-Caged Heptamethine Cyanine Switch Exhibits High Photostability for Bioimaging via Buffering Fluorogenicity”为题,于近日发表在CCS Chemistry上。该工作的共同第一作者为1818组博士后祁清凯博士和李锦博士,以上研究工作得到国家自然科学基金、我所创新基金等项目的资助。(文/图 祁清凯、乔庆龙)






